Zonder ontijzingsvloeistof geen vliegverkeer bij vriestemperaturen.
Want vliegtuigen bedekt met een ijslaagje kunnen immers niet meer veilig opstijgen.

Wat is die mysterieuze ontijzingsvloeistof dan wel?
Niet zo heel bijzonder.
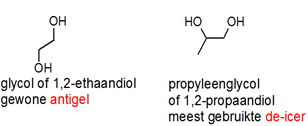
Ze is familie van glycol (1,2-ethaandiol).
Glycol is de vloeistof die aan het radiatorwater van auto’s wordt toegevoegd om te beletten dat de radiator en de leidingen in de winter open vriezen. Gewone anti-gel dus.
Tegenwoordig wordt bijna geen glycol-oplossing meer gebruikt voor de ontijzing van vliegtuigen.
Men is overgeschakeld naar een oplossing van het minder giftige 1,2-propaandiol, ook gekend als propyleenglycol
Als je propyleenglycol met water mengt in een 1:1-verhouding verkrijg je een oplossing die pas bij -40°C bevriest.
Als je zulke oplossingen op ijslagen spuit, verlaagt het stolpunt tot temperaturen ver beneden het stolpunt van water (0°C): het ijs wordt terug vloeibaar.
Hoe het komt dat propyleenglycol belet dat water niet bij 0°C bevriest, is een mooi en niet zo moeilijk chemie-verhaaltje dat ik jullie in deze laatste dagen van 2010 niet wil onthouden.
Als vloeibaar water ijs wordt, gaan de watermoleculen zich op een bijzondere wijze ten opzichte van elkaar rangschikken. Er ontstaat een ijl kristalrooster, met typische zeshoekige holten. Daardoor is ijs ijler (minder dicht) dan vloeibaar water. IJs drijft daarom ook op vloeibaar water.
De reden voor die ijle ijsstructuur ligt in de bouw van de watermoleculen en de wijze waarop die moleculen elkaar via zogenaamde waterstofbruggen aantrekken:
En nu komt het.
De de-icer moleculen, de propyleenglycolmoleculen hebben door hun bouw de mogelijkheid om met de watermoleculen ook waterstofbruggen te vormen.
Ze concurreren dus met de andere watermoleculen.
Ze beletten m.a.w. dat de kristalstructuur van ijs zich vormt, omdat ze als er als het ware tussen kruipen. Ze verbrodden de opbouw van die mooie ijsstructuur.
Water kan dus geen ijs worden. Water kan dus niet bevriezen.
En de vliegtuigen kunnen veilig opstijgen.
Zolang de voorraad 1,2-propaandiol strekt natuurlijk…
Zo zie je maar: chemie is overal, zelf op Brussels Airport.

Geen opmerkingen:
Een reactie posten